全球范围内,冠心病是人类首要致死原因。心脏支架植入术是治疗冠心病的重要手段,目前我国每年的心脏支架植入数量在百万枚以上。支架内血栓,尤其是晚期(1个月~1年)血栓,是心脏支架植入后的严重并发症。其发生率虽然低(0.6%~3%),但是致死率高(16.7%~33.8%),是目前心脏支架亟待解决的问题。
近日,广州医科大学附属第二医院(简称“广医二院”)心血管疾病研究所、心血管内科刘世明教授团队联合复旦大学附属中山医院葛均波院士团队对心脏支架内血栓的防治方法进行了多年的深入探索,最新合作研究成果“Identification of endothelial protein C receptor as a novel druggable agonistic target for reendothelialization promotion and thrombosis prevention of eluting stent”(内皮蛋白C受体作为新型药物激动靶点的鉴定,用于促进洗脱支架的再内皮化和预防血栓形成)发表在2024年11月的国际顶级期刊《Bioactive Materials》(医学一区)。
该研究得到国家自然科学基金和广东省、上海市、广州市等各级多个科研基金的支持,并已获得国家发明专利授权1项。广医二院为论文第一完成单位。通讯作者为刘世明教授、刘少军副研究员、复旦大学附属中山医院沈雳教授。葛均波院士及刘世明教授为项目资深专家(Senior authors)。刘少军副研究员为项目联系人(Lead contact)。陈静博士后、周昌颐硕士生、刘少军副研究员为论文共同第一作者。

记者了解到,该研究提出一个新的解决策略:立足于细胞差异化特征,确定关键的分子机制,从特异分子靶点的角度出发深入探索再内皮化延迟的具体原因,进而寻找心脏支架内晚期血栓的防治方法。再内皮化延迟是支架内晚期血栓形成的主要原因。寻求防止再狭窄和促进再内皮化之间的平衡是众多相关领域研究人员理想的心脏药物涂层支架的追求,也是国内外相关领域研究的热点和难点。
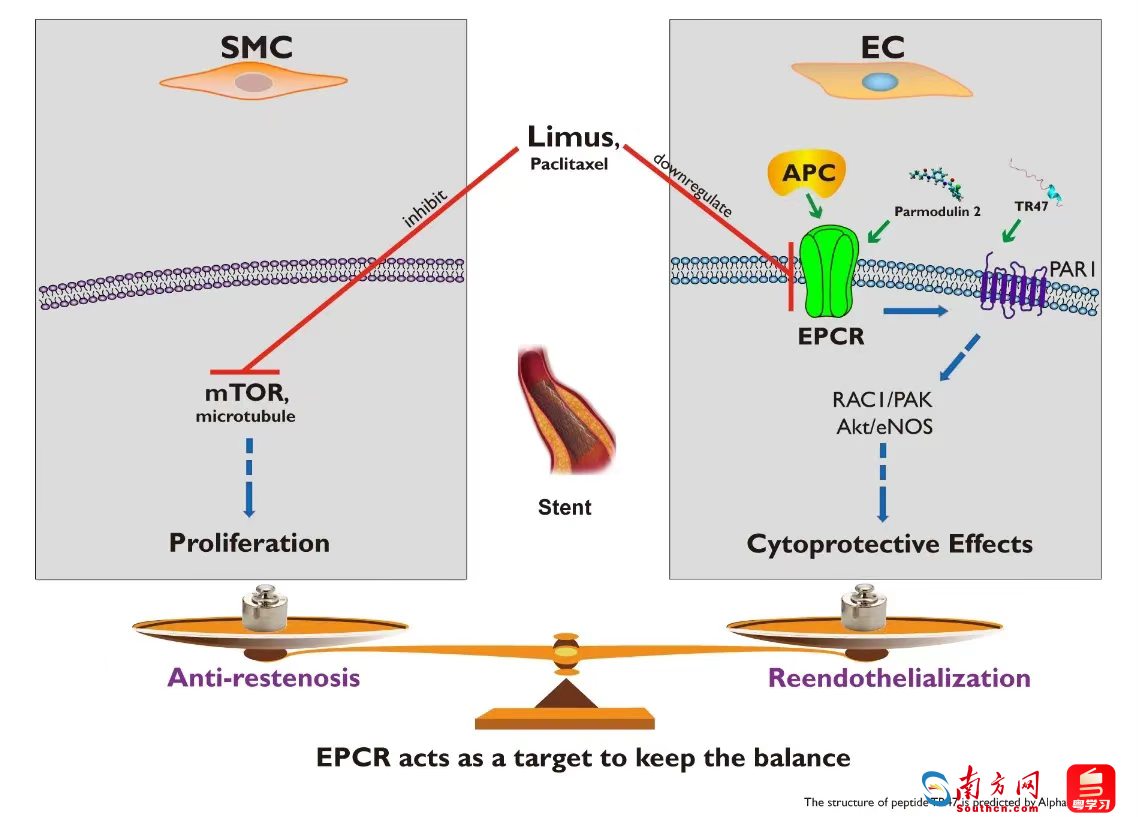
团队研究发现,在分子、细胞、模拟支架、支架体外环境等多个层面,通过其配体APC等方法激活血管内皮细胞特异性受体EPCR后,能够很好地发挥促进内皮化进程的作用。在动物实验中,无论是传统的金属支架,还是新型的可降解支架(从XINSORB®定制),APC新涂层均能有效地促进支架的再内皮化进程和抑制支架内血栓的形成。该研究发明的这种新型心脏支架能够有效地发挥防止再狭窄和抑制支架内血栓的双重效应。
南方网、粤学习见习记者 王子瑜










